
含氟有机化合物在医药、农业化学和材料科学中发挥着越来越重要的作用,含三氟甲氧基有机化合物便是其中一大类。由于三氟甲氧基具有强吸电子性和高脂溶性,因此在新药和农化产品中引入三氟甲氧基越来越多地引起了人们的关注。然而,含三氟甲氧基有机化合物的合成仍然是极具挑战性的工作,这主要是由于:(1)三氟甲氧基负离子容易分解;(2)过渡金属-三氟甲氧基复合物容易发生β-氟消除,至今还没有催化的对映选择性三氟甲氧基化反应的报道。
近期,南开大学化学院的汤平平教授课题组在Nature Chemistry上发表重要文章,报道了利用三氟甲基芳基磺酸酯(trifluoromethyl arylsulfonate,TFMS)作为新的三氟甲氧基化试剂,在银催化下实现了烯烃的分子间不对称溴-三氟甲氧基化反应。相比于其它三氟甲氧基化试剂,TFMS易于制备且比较稳定,具有良好的反应性。论文第一作者为郭硕。
汤平平教授。图片来源:南开大学
传统的三氟甲氧基化反应,如氯代前体的氯/氟交换、羟基化合物的亲电三氟甲基化反应等底物范围较窄,条件苛刻,往往要用到有毒试剂。Ngai等人曾发展了分子内OCF3迁移来制备三氟甲氧基化产物;Ritter等人发展了银催化的芳基锡或者芳基硼酸和三(二甲基氨基)鋶三氟甲氧基试剂TASOCF3的交叉偶联反应;卿凤翎等人发展了银催化的酚羟基或者醇羟基的氧化三氟甲基化反应来制备三氟甲基醚;刘国生等人发展了钯催化的利用AgOCF3对烯烃进行三氟甲氧基化得反应;张成潘等人发展了银催化的α-重氮酯的三氟甲氧基化反应,等等。所有以上三氟甲氧基化反应的方法都有各自的长处,但仍然存在各种局限性。如图1a所示,氟氧三氟甲烷FMT可以通过自由基过程进行三氟甲氧基化反应,但它是有毒气体且不便于操作;Noftle和Cady等人发展的三氟甲基三氟甲磺酸酯(Trifluoromethyl triflate,TFMT)可用于三氟甲氧基化反应,但它是挥发性液体(沸点仅19 ℃)限制了其应用。Langlois等人发展的2,4-二硝基三氟甲氧基苯反应性较差且底物范围窄。因此,仍然需要发展新的三氟甲氧基化试剂。
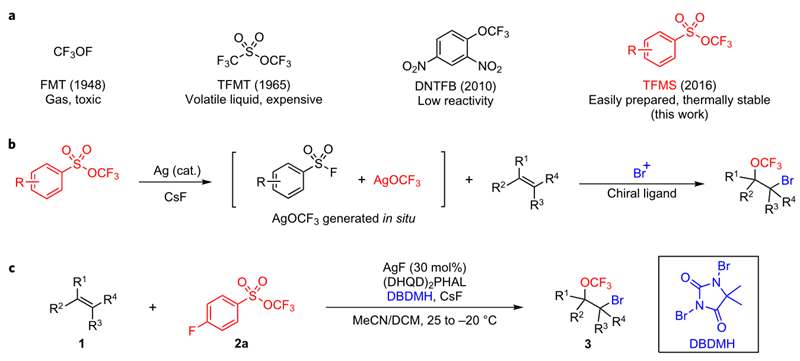
图1. 代表性的三氟甲氧基化试剂及TFMS的三氟甲氧基化反应。图片来源:Nature Chem.
受启发于Togni的发现,汤平平课题组利用Togni试剂和芳基磺酸便顺利制备了三氟甲基芳基磺酸酯TFMS,并将其作为新的三氟甲氧基化试剂,在银催化下原位产生AgOCF3,实现了对于烯烃的分子间不对称溴-三氟甲氧基化反应。
首先,作者以4-氟苯乙烯为底物,以1,3-二溴-5,5-二甲基乙内酰脲DBDMH为溴源,对于三氟甲氧基化试剂、添加剂银盐和氟盐、手性配体等都进行了考察,最终选定了AgF(30 mol%),手性配体L1(10 mol%),2.0当量CsF,3.0当量TFMS 2a,1.0当量DBDMH,在体积比为2:1的混合溶剂 MeCN/DCM中,氮气条件下反应能以较高的收率和选择性得到期望的溴-三氟甲氧基化反应产物(图2)。
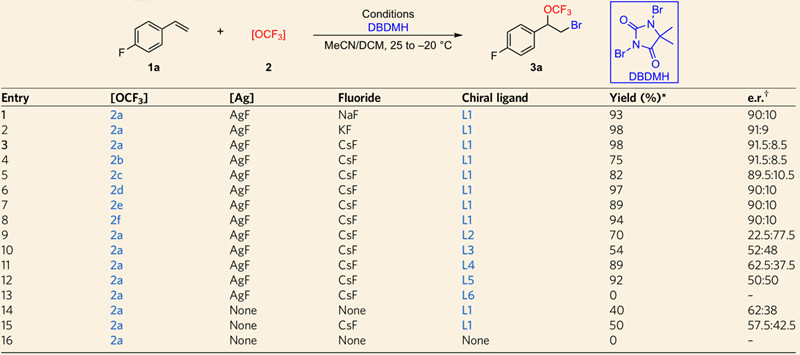
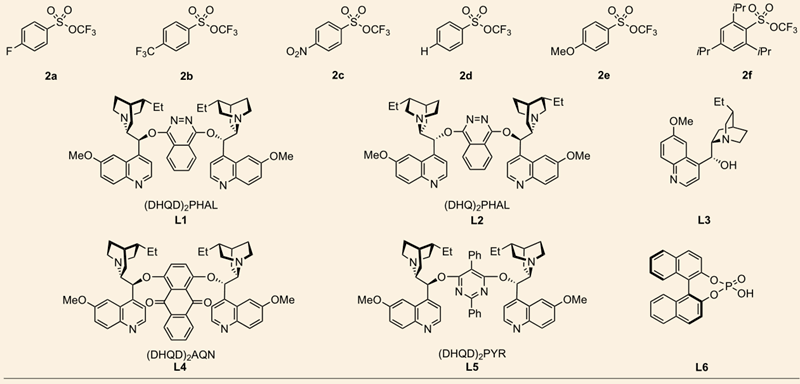
图2. 反应条件的筛选。图片来源:Nature Chem.
有了最佳反应条件,作者对反应底物进行了扩展。如图3所示,当苯乙烯的苯环上带有卤素、硝基、三氟甲氧基、氰基、酯基、烷基、内酯、杂环如三唑、咪唑等都可以兼容,能以优秀的收率和优良的选择性得到溴-三氟甲氧基化反应产物。除了苯乙烯,脂肪类的烯烃也能以良好的收率和立体选择性得到目标产物,除了端烯,脂肪链状内烯、环状烯烃也都可以得到良好的结果。一取代、二取代、三取代甚至四取代双键(3gg)都可以顺利发生反应。在富电子烯烃和缺电子烯烃共存的情况下,溴-三氟甲氧基化反应会发生在富电子烯烃上(3q, 3ee)。对于非环状烯烃,(E)-式双键(3v, 3x, 3bb)给出了和(Z)-式双键(1u, 1w, 1aa)相反的dr选择性。3i, 3t, 3x还通过单晶确定了其结构和立体化学,3r还能在克级规模以90%的收率和92.5:7.5的e.r.值得到,表明了该方法的实用性和可操作性。
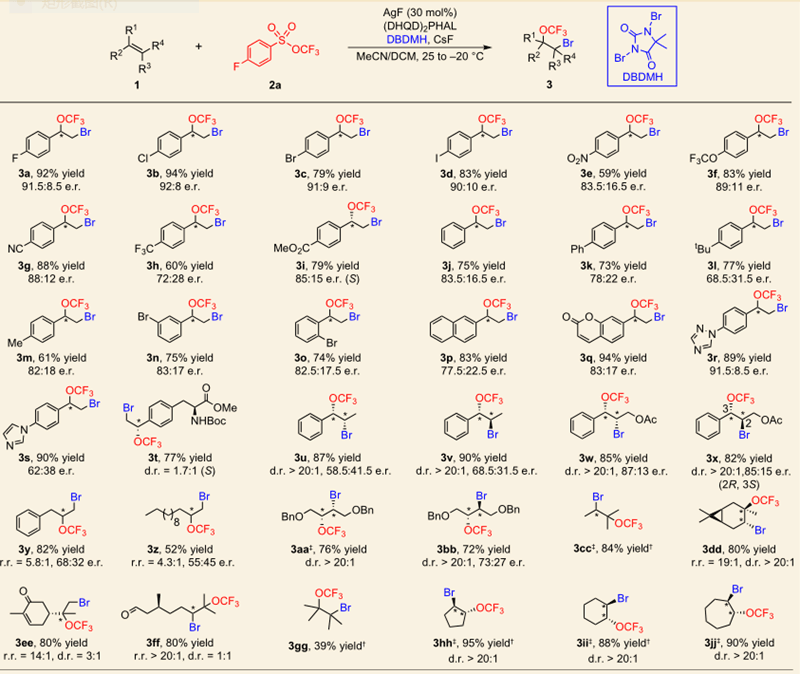
图3. 底物扩展一。图片来源:Nature Chem.
有了简单底物的成功,作者还在复杂底物上对该三氟甲氧基化反应进行了验证,如图4所示,三环、四环体系中的双键也都能以良好的收率得到所期望的产物,并由单晶确定其结构,但区域选择性(rr值)有所降低(5a, 5b)。另外,如金鸡纳碱、甾体、紫杉醇衍生物等复杂体系中的双键也能在标准条件下以中等到良好的收率得到溴-氟甲氧基化反应产物。
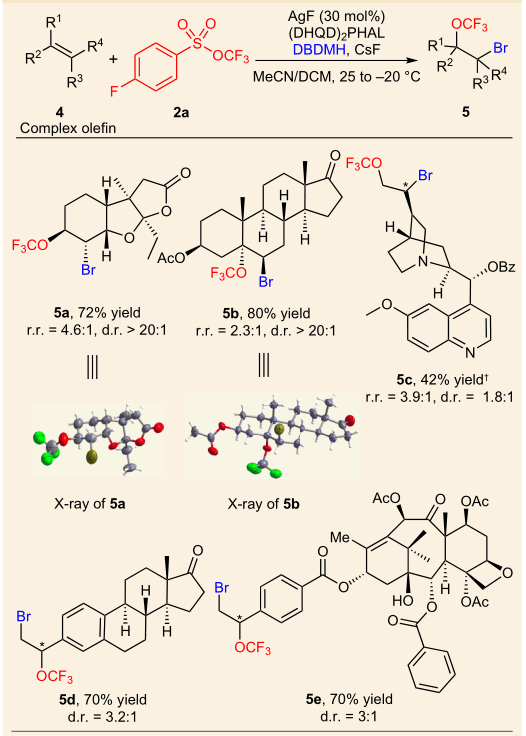
图4. 底物扩展二。图片来源:Nature Chem.
虽然该反应的机理还不甚清楚,但作者也通过19F NMR谱检测到反应体系中有AgOCF3 生成(7, ~25 ppm),并提出了反应可能的过渡态。如图5b所示,由于苯乙烯底物和手性配体中喹啉环的π,π-堆积作用,定位了底物在手性口袋中的位置,催化剂中的三级胺活化了DBDMH并导向了底物双键的溴代,而另一个喹啉氮原子和AgOCF3络合控制了三氟甲氧基化反应的位置和方向,具体细节还需要进一步的实验验证。
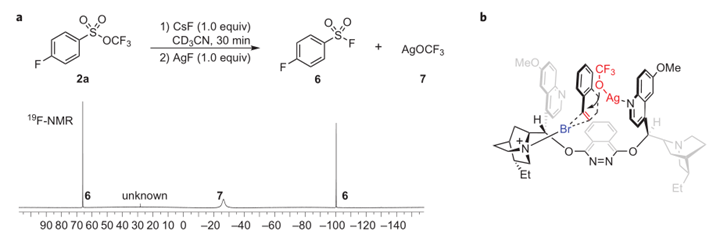
图5. 反应可能的过渡态。图片来源:Nature Chem.
—— 总结 ——
汤平平课题组利用三氟甲基芳基磺酸酯(TFMS)作为新的三氟甲氧基化试剂,在银催化下实现了烯烃的分子间不对称溴-三氟甲氧基化反应。TFMS易于制备且比较稳定,具有良好的反应性。该反应操作简便,在温和的条件下可以实现克级规模制备,底物适用性广泛,具有良好的官能团兼容性,可用于复杂天然产物或者天然产物类似物中双键的衍生化,在有机合成和药物改造中将有重要应用价值。